科室新闻
成果发表|宣武神外焦力群团队报道颈动脉狭窄患者年龄相关的解剖变化对CEA和CAS术后并发症的不同影响

首都医科大学宣武医院神经外科焦力群教授团队于2025年7月23日在《CNS Neuroscience & Therapeutics》杂志(2025 IF: 5.0,中科院1区期刊,JCR Q1区)在线发表题为“Age-Related Anatomical Changes in Carotid Artery Stenosis and Its Impact on Postoperative Complications in Stenting and Endarterectomy”的回顾性队列研究。
本研究证实了年龄相关的颈动脉解剖变化(包括颈总动脉直径增大、血管分叉位置上移及血管迂曲度增加)与颈动脉内膜切除术(CEA)和颈动脉支架置入术(CAS)术后并发症发生率显著相关,其中CAS手术结果受解剖因素影响更为明显,特别是症状性狭窄、主动脉弓变异等关键因素;基于这些特征建立的预测模型(AUC=0.82)能有效识别高风险患者,为临床实践提供了重要指导。宣武医院神经外科张潇医师、北京协和医学院周加博士生,宣武医院神经外科杨仁杰博士生为共同第一作者,宣武医院神经外科王韬副教授、焦力群教授、昆明医科大学第二附属医院闵晓黎教授为共同通讯作者。
关键词:年龄、解剖特征、颈动脉狭窄、动脉内膜切除术、术后并发症、支架
01、研究背景
颈动脉狭窄作为缺血性卒中的重要危险因素,其5年全因死亡率高达23.6%,目前临床主要采用CEA和CAS两种治疗方式。尽管CAS具有微创优势,但由于围术期卒中、心肌梗死等风险较高,其临床应用受到限制,特别是在高龄患者中表现更为显著:研究表明,70岁以上患者接受CAS后30天内卒中或死亡风险明显高于CEA,而CEA虽在神经系统结局上表现稳定,却伴随高龄患者死亡率上升的问题。年龄因素不仅影响治疗选择,更与颈动脉解剖结构改变密切相关,如血管直径增大、分叉位置变化和血管迂曲度增加等,这些变化可能增加CAS操作难度和栓塞风险,但目前尚缺乏系统的研究来阐明这些解剖特征如何介导年龄与术后并发症之间的关系。为此,该研究创新性地将年龄相关的颈动脉解剖学特征纳入预测模型,通过量化血管重塑指标(包括颈总动脉直径、分叉距离和迂曲度等),旨在建立更精准的个体化风险评估体系,为临床治疗决策提供新的解剖学依据,从而优化手术方案选择,提高患者预后。
02、研究方法
本研究采用单中心回顾性队列设计,遵循STROBE报告规范,纳入2020年1月至2021年11月期间429例接受CEA或CAS的颈动脉狭窄患者(图1)。研究系统采集了患者人口学特征、合并症及术后30天内并发症,重点测量了颈总动脉直径、颈内动脉近远端直径、分叉位置、血管迂曲度等解剖学参数,同时评估主动脉弓分型和钙化程度等血管特征。采用多变量logistic回归、决策树、支持向量机、随机森林和梯度提升机,分别建立并发症预测模型,并通过ROC曲线、校准曲线和决策曲线分析验证模型的预测效能和临床适用性。
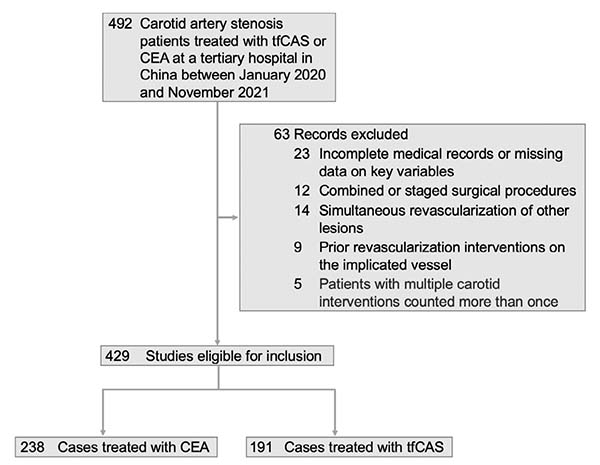
图1 研究人群筛选流程图
03、研究结果
该研究共纳入429例有详细手术记录的患者,其中191例接受CAS,238例接受CEA。研究发现,年龄增长与特定的颈动脉解剖学改变存在显著关联(表1),主要表现为颈总动脉直径增大(尤其右侧)、锁骨至分叉处距离缩短、颈总动脉和颈内动脉迂曲度增加。同时,人体参数对解剖特征的影响呈现特异性模式:身高主要影响血管走行距离(如锁骨至分叉距离)和迂曲度,体重显著影响颈总动脉和颈内动脉直径。这些发现为个体化手术方案制定提供了重要的解剖学依据。
这些血管形态学改变在两种手术方式中均显示出与术后并发症发生率的显著相关性。在CAS患者中,症状性狭窄、主动脉弓解剖变异、CCA开口病变以及CCA直径等指标被确认为并发症的独立预测因子(p<0.05)。基于这些解剖学特征建立的预测模型展现出良好的判别效能,其AUC达到0.82,为临床风险评估提供了可靠工具(图2)。与CAS不同,症状性狭窄是CEA组并发症的唯一重要预测因素。这种差异源于两种术式的本质区别:CAS高度依赖血管解剖条件,在迂曲钙化血管中操作风险倍增;而CEA通过直接暴露手术区域,能有效规避解剖变异带来的挑战。中国患者的血管解剖特征呈现独特复杂性,表现为III型主动脉弓比例更高(28.9% vs 全球数据)、血管钙化程度更重以及颈动脉迂曲指数更大。这些特征使CAS手术难度显著增加,尤其对老年患者影响更为突出。
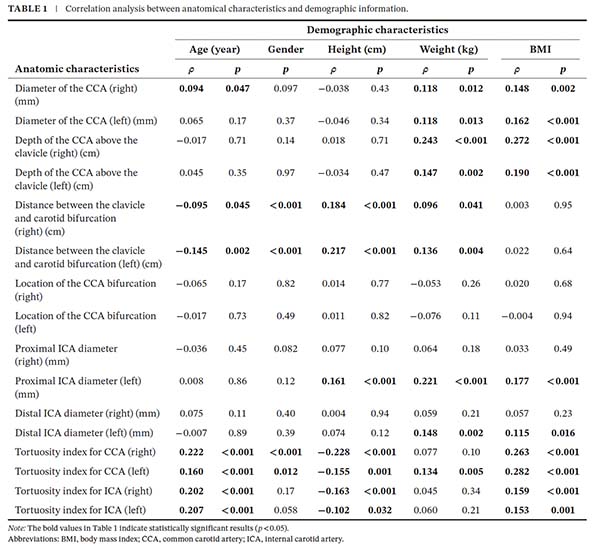
表1 解剖学特征与人口统计学信息的相关性分析
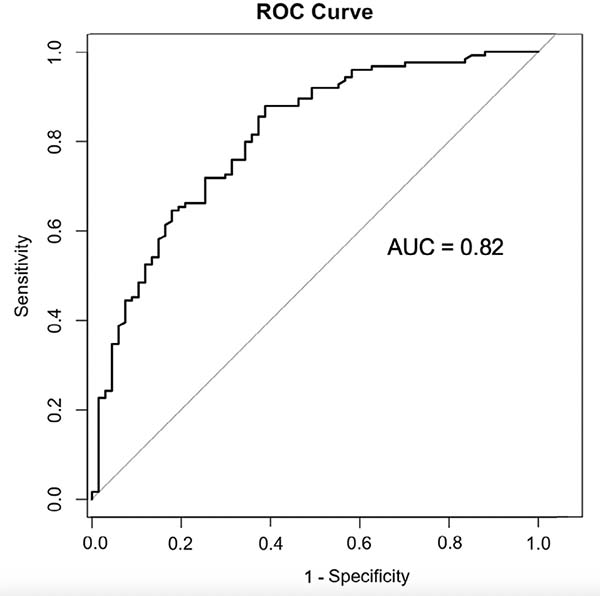
图2 颈动脉支架置入术后并发症预测模型ROC曲线
04、研究结论及临床意义
研究发现,颈动脉解剖结构随年龄增长呈现显著改变,表现为血管增宽、迂曲和钙化等特征。这些血管重塑特征与CAS术后并发症风险密切相关,但在CEA患者中未发现类似关联,凸显两种术式对解剖条件的依赖性差异:CAS高度依赖血管解剖条件,在迂曲钙化血管中操作风险倍增;而CEA通过直视下斑块清除,能有效规避解剖变异带来的挑战。研究结果具有三重临床价值:一是为高龄患者术式选择(CEA/CAS)提供解剖学依据;二是通过术前评估血管特征(如颈总动脉直径、迂曲度)预测并发症风险;三是指导CAS术中针对复杂解剖进行技术调整。特别值得注意的是,中国患者存在III型主动脉弓比例高、血管钙化程度重等特征,更需个体化评估选择血运重建策略。这些发现为优化手术方案、改善患者预后提供了重要指导。

第一作者
张潇
首都医科大学宣武医院
神经外科 医师
医学博士,师从焦力群教授;首都医科大学-英国牛津大学联合培养博士。主持四大慢病国家科技重大专项青年人才培育计划1项,迄今以第一/共一作者在Stroke、Ageing Research Review、Aging Dis、JNIS、TSR、Cochrane Reviews等期刊发表SCI论文30篇,参编书籍2部,获得专利授权3项。

共同第一作者
周加
北京协和医学院(清华大学医学部)八年制2018级
以一作及共同一作身份发表SCI论文16篇,获国家发明专利及实用新型4项,主持国家级大学生创新训练项目1项。
共同第一作者
杨仁杰
首都医科大学宣武医院
在读博士研究生
师从焦力群教授。主要研究方向为缺血性脑血管病的外科和介入治疗。于JNIS,EJVES等杂志发表SCI文章4篇。

通讯作者
首都医科大学宣武医院副院长
主任医师 教授 博士生导师
首都医科大学宣武医院副院长,介入放射科主任,神经外科副主任,脑血运重建中心主任,国家区域医疗中心、宣武医院济南医院院长。兼任《中国脑血管病杂志》主编;中国医师协会神经介入专业委员会副主委;国家卫健委继教中心神经介入专委会主委;国家卫健委脑防委缺血性卒中外科专委会主委;国家卫健委脑防委缺血性卒中介入专委会副主委;北京介入医学会副会长等职务。毕业于山东医科大学,先后师从于朱树干教授和凌锋教授,获得神经外科硕士和博士学位,并在鲍圣德教授的指导下,在北京大学完成博士后研究。从事缺血性脑血管病的外科和介入治疗,在国际上率先开展了复合手术治疗颈动脉闭塞、椎动脉闭塞,以及药物球囊治疗椎动脉狭窄等创新手术,并带领宣武医院脑血运重建中心在此领域深入研究,同时,长期重视教育培训,为中国培养了大批高水平的医生。
【出诊时间:每周三上午(介入放射科) 每周一下午(特需介入放射科)】

共同通讯作者
闵晓黎
昆明医科大学
教授 博士生导师
医学博士,新西兰奥克兰大学博士后。博士后流动站导师。云南省精准神经外科团队方向带头人,中青年学科带头人乘风计划人才,科技创新之星。中国解剖学会临床神经解剖分会常委、云南省康复医学会脑血管病专业委员会副主任委员、云南省医院协会心脑同治专业委员会副主任委员等。主持国家自然科学基金等国家级课题4项、省部级课题13项,以第一/通讯作者在Redox Biol、FASEB J、TSR、Mol Neurobiol等期刊发表SCI论文30余篇,主编书籍12部,获得专利授权8项,软著登记权6项。

共同通讯作者
王韬
首都医科大学宣武医院
神经外科主治医师 副教授
副研究员 硕士生导师
青年学者博士生导师
毕业于北京协和医学院(清华大学医学部)临床医学八年制。致力于颅内动脉狭窄、颈动脉狭窄和烟雾病等缺血性脑血管病的外科、介入及复合手术的诊疗。北京市科技新星,中国科协战略发展部科技智库青年人才,北京市医药卫生科技创新成果转化专家库入库专家,首都医科大学优秀青年人才。迄今以第一/通讯作者在JAMA、Stroke、Ageing Research Review, Aging and Disease、SVN、JNIS、Cochrane Reviews等期刊上发表SCI论文50余篇,参编书籍2部,获得专利授权8项。主持国家自然科学基金、北京市自然科学基金等9项课题。《Brain Circulation》和《中国脑血管病杂志》青年编委。北京医师协会神经介入专科青年医师分会理事,北京神经科学学会神经介入专业委员会委员,中国医药教育协会脑卒中血运重建专业委员会常务委员兼副秘书长,中国志愿医生。





















